- +1
《科學(xué)》:新型抑制劑有望治療神經(jīng)退行性疾病
原創(chuàng) 圖圖 神經(jīng)現(xiàn)實(shí)
文獻(xiàn):Yan, Jing, et al. "Coupling of NMDA receptors and TRPM4 guides discovery of unconventional neuroprotectants." Science 370.6513 (2020).
DOI:https://doi.org/10.1126/science.aay3302
導(dǎo)讀作者:圖圖 | 封面:Curtis Cripe
N-甲基-D-天門(mén)冬胺酸受體(N-methyl-D-aspartate receptor,NMDAR)是眾所周知的離子型谷氨酸受體,可介導(dǎo)鈉離子、鈣離子等的跨膜運(yùn)輸。他們不僅對(duì)大腦的發(fā)育及突觸可塑性調(diào)節(jié)至關(guān)重要,對(duì)記憶及獲得性神經(jīng)保護(hù)等適應(yīng)性機(jī)制的加固也是必不可少的。
然而,天使與惡魔同在,NMDAR也有著鮮為人知的黑暗面-中斷遺傳物質(zhì)轉(zhuǎn)錄、導(dǎo)致線(xiàn)粒體罷工,更甚能引起興奮性神經(jīng)元中毒及死亡。直到如今,我們也并不清楚他是如何在這兩種“人格”中游走,為何他會(huì)對(duì)一心要保護(hù)的神經(jīng)元下此毒手?

近日來(lái)自德國(guó)海德堡大學(xué)的科學(xué)家們?cè)赟cience雜志上發(fā)表了他們的研究,他們致力于尋找NMDAR與細(xì)胞凋亡之間的結(jié)構(gòu)基礎(chǔ),發(fā)現(xiàn)NMDAR獲得毒物的特質(zhì)是因?yàn)榕c瞬態(tài)感受器電位陽(yáng)離子通道子類(lèi)M的4號(hào)成員(TRPM4)之間發(fā)生相互作用形成復(fù)合體,而并不是大眾之前所認(rèn)為的細(xì)胞內(nèi)高鈣離子負(fù)荷。所以,他們猜想如果能破壞NMDAR/TRPM4 (N/T)之間的聯(lián)系,也許能夠消除NMDAR引起的細(xì)胞毒性減少神經(jīng)元的傷亡。
接下來(lái),他們以結(jié)構(gòu)為基礎(chǔ)進(jìn)行計(jì)算藥物篩選,發(fā)現(xiàn)TRPM4細(xì)胞內(nèi)結(jié)構(gòu)域只有57個(gè)氨基酸的TwinF對(duì)N/T聯(lián)系至關(guān)重要,無(wú)論表達(dá)TwinF或者利用基于TwinF結(jié)構(gòu)篩選出的抑制劑小分子都可以在不破壞NMDAR和TRPM4離子通道的基礎(chǔ)上,解除他們之間的關(guān)聯(lián),最終達(dá)到恢復(fù)遺傳物質(zhì)轉(zhuǎn)錄、線(xiàn)粒體正常工作等保護(hù)細(xì)胞的功效。這項(xiàng)新研究為一直以來(lái)很難有效治療的神經(jīng)退行性疾病提供了新的攻克方向。
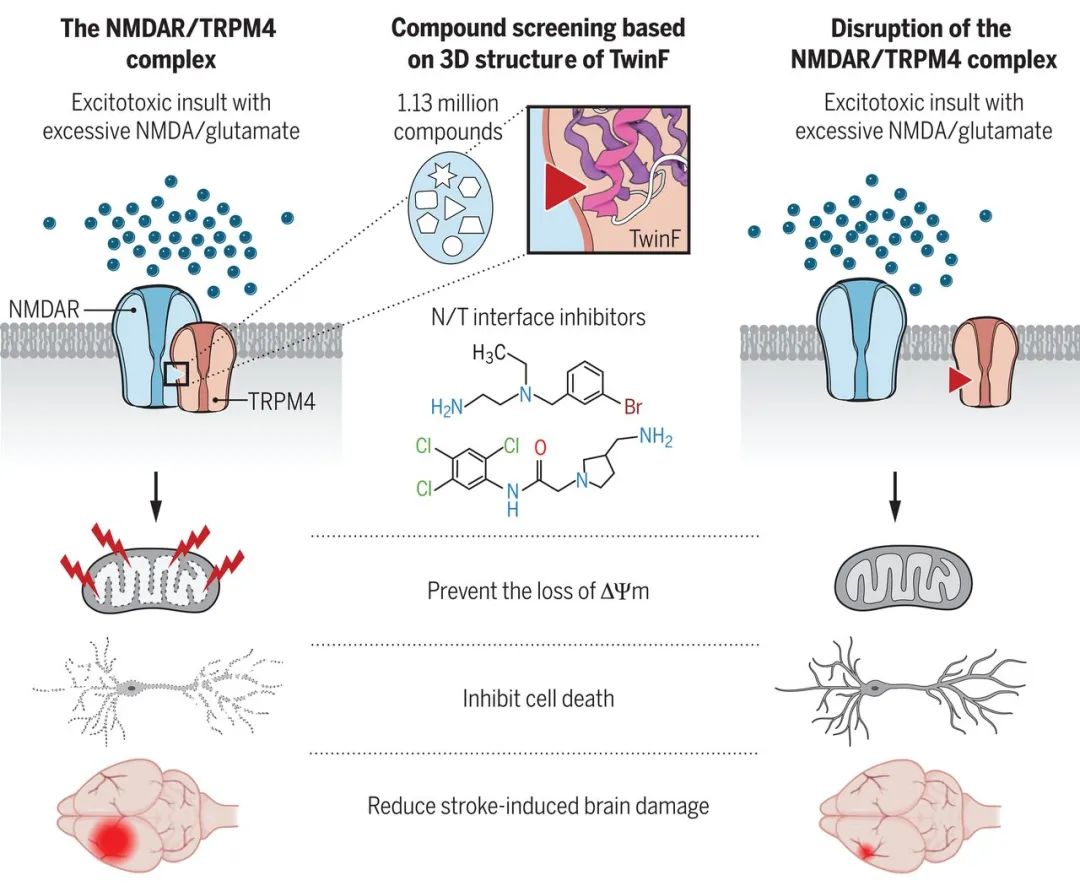
- Yan et al., Science -
本文為澎湃號(hào)作者或機(jī)構(gòu)在澎湃新聞上傳并發(fā)布,僅代表該作者或機(jī)構(gòu)觀(guān)點(diǎn),不代表澎湃新聞的觀(guān)點(diǎn)或立場(chǎng),澎湃新聞僅提供信息發(fā)布平臺(tái)。申請(qǐng)澎湃號(hào)請(qǐng)用電腦訪(fǎng)問(wèn)http://renzheng.thepaper.cn。





- 報(bào)料熱線(xiàn): 021-962866
- 報(bào)料郵箱: news@thepaper.cn
滬公網(wǎng)安備31010602000299號(hào)
互聯(lián)網(wǎng)新聞信息服務(wù)許可證:31120170006
增值電信業(yè)務(wù)經(jīng)營(yíng)許可證:滬B2-2017116
? 2014-2025 上海東方報(bào)業(yè)有限公司




